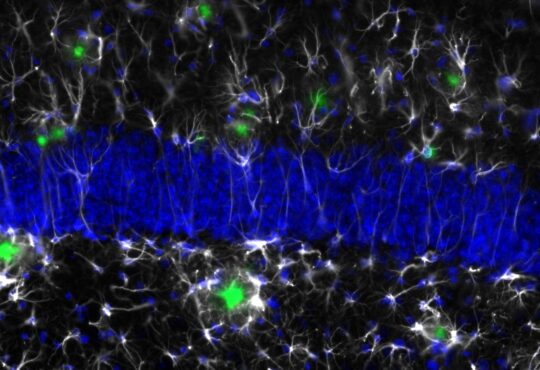
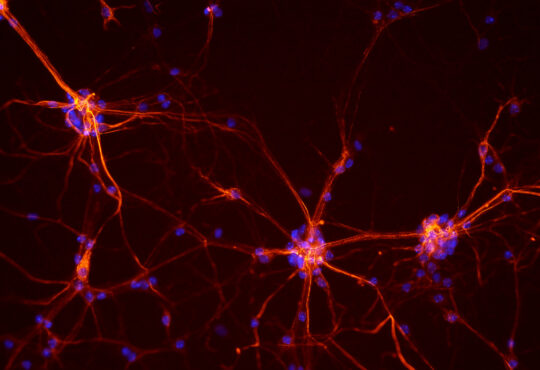
Nuovi target terapeutici e diagnostici per le malattie neurodegenerative
Lo studio delle anomalie mitocondriali nelle cellule e sul loro ruolo nella morte cellulare potrebbe aiutare a capire come contrastare le malattie neurodegenerative.
RICERCANDO ALL’ESTERO – “Non ci sono cure per le malattie neurodegenerative ed essendo patologie che stanno aumentando in modo esponenziale in tutto il mondo, ce n’è un estremo bisogno. Scoprire come le cellule del nostro cervello muoiono è un modo per bloccare lo sviluppo di queste malattie. E poi, ho sempre desiderato fare qualcosa di tangibile per aiutare la gente e ora faccio una scienza concretamente utile alla popolazione”.
 Nome: Silvia Fossati
Nome: Silvia Fossati
Età: 39 anni
Nata a: Montevarchi (AR)
Vivo a: New York (Stati Uniti)
Dottorato in: Farmacologia (Firenze)
Ricerca: Il danno vascolare nell’Alzheimer e nuovi biomarcatori per le malattie neurodegenerative.
Istituto: Department of Neurology, Department of Psychiatry, New York University School of Medicine (USA)
Interessi: cucinare, fare dolci, teatro, danza, high tea con le mie amiche.
Di New York mi piace: è piena di persone diverse, ti dà tantissime possibilità.
Di New York non mi piace: c’è troppo stress, si lavora troppo, si va sempre di corsa.
Pensiero: Perfection is not attainable, but if we chase perfection we can catch excellence. (Vince Lombardi)
I meccanismi molecolari alla base di molte malattie neurodegenerative come l’Alezheimer e il Parkinson o del disturbo post-traumatico da stress e del trauma cerebrale non sono ancora del tutto compresi. Lo stress cellulare, la morte programmata per apoptosi e l’infiammazione sono processi che svolgono un ruolo fondamentale nello sviluppo di queste patologie: sempre più, la ricerca mirata a individuare sia composti farmacologici in grado di inibire questi eventi sia nuovi biomarcatori da usare in fase diagnostica giocano un ruolo cruciale nell’affrontare tali malattie.
Qual è il contributo del danno vascolare nello sviluppo dell’Alzheimer?
In quasi l’80% dei malati di Alzheimer si è visto che attorno ai vasi cerebrali c’è un deposito di beta amiloide, la principale proteina coinvolta nell’Alzheimer. Questa condizione compromette la circolazione del sangue all’interno dei vasi, può causare ischemia cerebrale e tutta una serie di danni che si trasmettono ai neuroni e portano al declino cognitivo e alla demenza tipici di questa malattia. Poiché sembra essere un danno abbastanza precoce, la deposizione di beta amiloide attorno a vene, capillari e arterie è sempre più riconosciuta come un importante fattore nella patogenesi dell’Alzheimer.
La mia ricerca si interessa in particolare delle anomalie mitocondriali delle cellule dei vasi sanguigni, dei neuroni e delle cellule gliali, e sul loro ruolo nella morte cellulare. I mitocondri sono organelli che producono energia e reagiscono alla proteina amiloide smettendo di produrre energia e attivando una cascata di segnali che inducono alla morte della cellula.
Abbiamo visto che questo meccanismo molecolare è innescato da alcuni recettori di membrana chiamati death receptor (DR), i quali si legano all’amiloide e attivano la cascata delle caspasi che dà inizio all’apoptosi (cioè al processo di morte cellulare programmata). In particolare ci sono due recettori coinvolti, il DR4 e DR5: normalmente, questi recettori sono attivati da una molecola messaggero di nome TRAIL ma sembra che beta amiloide riesca a formare degli oligomeri, cioè gruppi di proteine aggregate tra loro, riconosciuti al posto di TRAIL. Il legame con beta amiloide attiva il recettore che recluta la prima caspasi (Cas 8) e porta alla morte della cellula.
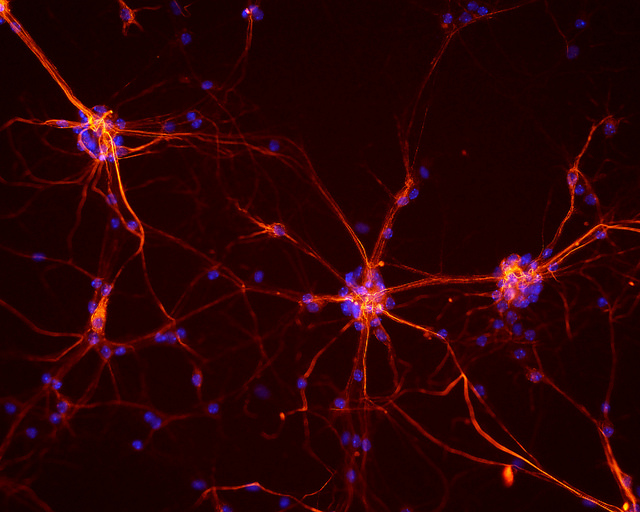
È possibile bloccare l’apoptosi di queste cellule per impedire lo sviluppo della demenza?
Esistono in commercio dei farmaci in grado di bloccare il danno mitocondriale: si tratta di composti approvati per l’uso clinico da parecchi anni per malattie completamente diverse, come il glaucoma, l’epilessia e la prevenzione della malattia da altitudine. Si chiamano inibitori dell’anidrasi carbonica e dai primi risultati, ancora molto preliminari, sembra siano efficaci anche nel ridurre gli effetti dei depositi di amiloide nell’Alzheimer.
L’anidrasi carbonica è un enzima presente normalmente nelle cellule, anche a livello mitocondriale, che trasforma anidride carbonica e acqua in acido carbonico e protoni. Abbiamo visto che, inibendo l’anidrasi carbonica, si inibiscono tutta una serie di processi tossici attivati dalla proteina amiloide, come la produzione di acqua ossigenata, le alterazioni nel potenziale di membrana mitocondriale, il rilascio di citocromo C, l’attivazione delle caspasi e l’apoptosi. Inoltre, da studi comportamentali sugli animali, abbiamo osservato un miglioramento della memoria in seguito all’assunzione di questi farmaci. Ovviamente servono ulteriori esperimenti, ma se questi composti veramente funzionano, proseguiremo con studi clinici sull’uomo, che dovrebbero essere più rapidi essendo farmaci già approvati dalla FDA (Food and Drug Administration).
Per quanto riguarda la diagnosi, invece?
Un altro aspetto del mio lavoro comprende la ricerca di biomarcatori, cioè molecole in grado di segnalare una malattia, nei fluidi corporei e in particolare nel sangue. I migliori marcatori per l’Alzheimer sono la proteina beta amiloide e tau, un’altra proteina neuronale espressa in forma patologica. Tuttavia, con le tecniche di analisi classiche come l’ELISA (basata sull’interazione tra un anticorpo fluorescente e la proteina bersaglio) non si riusciva a individuarle perché i loro livelli nel sangue erano troppo bassi. Noi usiamo una nuova tecnologia, chiamata Simoa, dotata di particolari microchip e in grado di “vedere” praticamente un singolo legame proteina-anticorpo tramite delle micro palline magnetiche.
Grazie a Simoa, siamo riusciti a misurare i livelli di tau nel sangue di pazienti con Alzheimer e a verificare che, in caso di malattia, questa proteina è over espressa.
Abbiamo applicato lo stesso metodo anche a tutti quei disturbi legati a qualche trauma cerebrale: tau, infatti, è una proteina che viene rilasciata poche ore o al massimo giorni dopo un trauma e, in genere, col tempo ritorna a livelli normali. Se si accumula e crea depositi anomali può portare a malattie simili al Parkinson o all’Alzheimer.
Da qualche anno, lavoro anche al Cohen Veteran Center dove mi occupo di trauma cranico e disturbo post-traumatico da stress. L’obiettivo della ricerca è capire se un numero ripetuto di traumi cerebrali o un trauma cerebrale particolarmente severo (comune sia ai veterani di guerra sia a certi tipi di atleti) causa un rialzo di tau a lungo termine (10-20 anni) e se questo possa indurre malattie come l’Encefalopatia Traumatica Cronica (conosciuta come la demenza dei pugili).
I marcatori che stiamo studiando sono quelli che appartengono all’asse HPA (ipotalamo-ipofisi-surrene), come il cortisolo e l’ormone di rilascio della corticotropina, e quelli coinvolti nell’infiammazione, come IL6, IL10 e TNF alfa.
Per adesso il tutto a scopo diagnostico, ovvero come indicatori dell’efficienza di un trattamento, che al momento purtroppo consiste principalmente in supporto psicologico.
Uno dei miei collaboratori sta mettendo a punto una particolare PET (Positron Emission Tomography) per misurare il livelli di tau nel cervello di pazienti vivi. È una cosa che viene già fatta per l’amiloide nell’Alzheimer, ma fino allo scorso anno non c’erano traccianti radioattivi in grado di interagire con tau.
Quali sono le prospettive future del tuo lavoro?
Per quanto riguarda gli inibitori di proteasi, continuare gli studi per confermare la loro efficacia in modo da poter disegnare un trial clinico sull’uomo.
Per la ricerca sul trauma cranico, l’idea principale è individuare un gruppo di marcatori da misurare nel sangue di veterani di guerra o sportivi che hanno subito un danno, per verificare se è diventato cronico e quindi se c’è il rischio di sviluppare una malattia neurodegenerativa. Tra l’altro se troviamo biomarcatori validi possiamo pensare anche a una terapia efficace.
Leggi anche: Un freno per la memoria a lungo termine
Pubblicato con licenza Creative Commons Attribuzione-Non opere derivate 2.5 Italia. ![]()