Microscopia a super risoluzione per lo studio del sistema nervoso
Gli approcci di microscopia a super risoluzione hanno creato nuove possibilità per comprendere la struttura e la funzione delle cellule.
RICERCANDO ALL’ESTERO – “Lo sviluppo dei metodi di imaging sta rivoluzionando la nostra capacità di vedere i processi biologici e l’organizzazione cellulare anche a scale molto piccole. La microscopia a super risoluzione ha permesso di visualizzare meglio le cose ed è un campo nuovo, in cui è ancora tutto da scoprire. Seeing is believing”.
 Nome: Elisa D’Este
Nome: Elisa D’Este
Età: 32 anni
Nata a: Udine
Vivo a: Gottingen (Germania)
Dottorato: nanotecnologie (Trieste)
Ricerca: Periodicità del citoscheletro subcorticale nel sistema nervoso
Istituto: Department of NanoBiophotonics, Max Planck Institute for Biophysical Chemistry (Gottingen, Germania)
Interessi: viaggiare, andare a concerti, ho fondato una startup (GeniusChoice)
Di Gottingen mi piace: c’è molto verde, è una città giovane
Di Gottingen non mi piace: è piccola, se c’è brutto tempo non c’è molto da fare
Pensiero: “Nothing venture, nothing win.” (Edmund Hillary)
La microscopia ha sempre svolto un ruolo chiave nella biologia cellulare. I progressi tecnici e di fabbricazione hanno migliorato notevolmente la qualità delle immagini, ma alla fine si sono scontrati con il limite della risoluzione. I nuovi approcci di super risoluzione, basati su una particolare illuminazione del campione, sulla risposta non lineare dei fluorofori e sulla precisa localizzazione di singole biomolecole, hanno creato nuove possibilità per studiare la struttura e la funzione delle cellule.
Come funzionano i microscopi a super risoluzione?
Nel laboratorio dove lavoro usiamo una particolare tecnica chiamata STED (Stimulated Emission Depletion Microscopy) basata sulla fluorescenza. In generale i microscopi a fluorescenza sfruttano molecole colorate, dette fluorofori, per marcare specifici componenti cellulari e permettono di osservare in tempo reale le strutture all’interno di un campione. Il limite di questa tecnica sta nella bassa risoluzione spaziale: a causa della diffrazione della luce, il limite fisico di ingrandimento è dato dalla metà della lunghezza d’onda della luce usata e per la microscopia a fluorescenza convenzionale è di 200 nm. Questo significa che se due strutture cellulari sono distanti meno di 200 nm, un microscopio normale non è in grado di vederle come distinte.
La STED è in grado di superare questo limite e di raccogliere immagini con una risoluzione di addirittura 20 nm. La tecnica è stata sviluppata dal mio capo, Stefan Hell, che nel 2014 ha vinto il premio Nobel per la chimica.
La novità sta nell’usare due fasci di luce laser per illuminare il campione: il primo eccita le molecole e tutte quelle che si trovano all’interno dello spot luminoso iniziano ad emettere fluorescenza; il secondo, a forma di ciambella, spegne le molecole più in periferia lasciando “acceso” un diametro di pochi nanometri. In pratica si tratta di un gioco on/off grazie al quale possiamo migliorare la risoluzione di un certo sistema.
In genere il termine microscopia a super risoluzione non è molto usato e si preferisce parlare di nanoscopia.
Che tipo di sistemi studi?
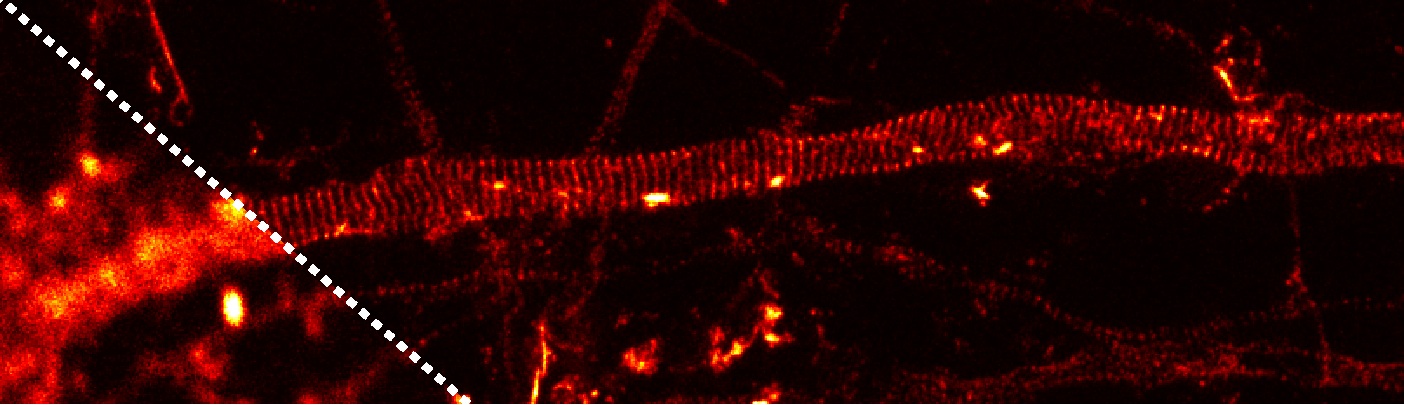
Mi occupo del citoscheletro dei neuroni, in particolare delle strutture sottocorticali che si trovano subito al di sotto della membrana cellulare. Circa due anni fa, sia il mio gruppo sia alcuni ricercatori di Harvard hanno dimostrato che in questa zona c’è una struttura di actina e spettrina con una periodicità di 190 nm che avvolge l’intero assone. Essendo questa distanza inferiore al limite di risoluzione delle tecniche convenzionali, la sua visualizzazione non sarebbe stata possibile nemmeno con il migliore microscopio confocale del mondo, ma necessitava appunto di un approccio nanoscopico.
Questo è uno di quei casi in cui lo sviluppo tecnico e la conoscenza biologica sono andati in parallelo. Era già noto che actina e spettrina sono proteine importanti per i neuroni, che la spettrina è espressa negli assoni e che ci sono diversi tipi di spettrina in diverse zone dell’assone: quello che non si conosceva era l’organizzazione di queste molecole. Usando i microscopi a super risoluzione e combinando vari campioni, si è visto che la loro distribuzione non omogenea ma che c’è uno schema periodico fatto di anelli di actina collegati da ponti di spettrina.
Quali sono le funzioni di questa struttura?
Non tutte sono ancora chiare. Per ora è certo che giochi un ruolo strutturale-meccanico nei neuroni: mutanti del verme nematode Caenorhabditis elegans in cui la spettrina non funziona mostrano una particolare fragilità negli assoni, che si spezzano facilmente. Il fatto non ci ha sorpreso più di tanto. Pensiamo ai nervi che corrono lungo una gamba o un braccio: non è che gli assoni si rompono quando li pieghiamo!
Inoltre sembra che questo schema actina-spettrina influenzi l’organizzazione di altre proteine, per esempio quelle di adesione e i canali sodio-potassio.
Abbiamo anche verificato la sua presenza nelle fasi di sviluppo dei neuroni in vitro: dai nostri esperimenti è emerso che già due giorni dopo la messa in coltura, quando il neurone ha deciso quale sarà l’assone, queste strutture sono visibili. Se siano o meno presenti anche prima è difficile da capire, forse anche per una questione puramente tecnica. I filamenti di actina sono tantissimi e le strutture sono molto scure rispetto ad altri componenti cellulari per cui potrebbero semplicemente essere nascoste da elementi superficiali più luminosi.
Un’altra scoperta interessante è che la localizzazione di questi anelli actina-spettrina non è limitata ai neuroni dell’ippocampo ma sono ubiquitari sia nel sistema nervoso centrale sia in quello periferico. E non avvolgono solo gli assoni ma anche i dendriti, seppur con una struttura più complicata e con funzioni ancora da investigare.
Infine, la struttura è presente anche in altre cellule cerebrali come gli oligodendrociti.
Cosa succede a questa zona del citoscheletro durante la formazione della mielina?
In generale, il processo di mielinizzazione provoca grossi riarragiamenti nel citoscheletro ed eravamo curiosi di vedere cosa succede nelle regioni sottocorticali. I risultati che abbiamo ottenuto mostrano che le strutture actina-spettrina rimangono inalterate, le ritroviamo anche sotto la mielina e probabilmente coordinano tutto il processo. Infatti, a livello dei nodi di Ranvier, interruzioni della guina mielinica, dove c’è una forte interazione tra la cellula gliale e l’assone, i due citoscheletri sono allineati. Ora che abbiamo capito l’organizzazione di questo tipo di citoscheletro nel nodo di Ranvier, ci concentreremo sul suo significato e sulla sua funzione.
Quali sono le prospettive future del tuo lavoro?
Mi piacerebbe riuscire a capire il nesso tra le alterazioni di questa struttura citoscheletrica e tutta una serie di patologie: ci sono diverse indicazioni sul fatto che mutazioni a carico delle proteine coinvolte possono causare malattie, come atassia, sclerosi multipla o altre patologie neurodegenerative. Se le mutazioni siano la causa o la conseguenza e quale sia l’effetto è ancora da studiare.
Se penso molto a lungo termine, dato che per ora faccio ricerca di base, mi piacerebbe lavorare su queste strutture per mitigare gli effetti delle patologie e magari addirittura prevenirle.
Leggi anche: Il nobel per la chimica l’ha vinto l’infinitamente piccolo
Pubblicato con licenza Creative Commons Attribuzione-Non opere derivate 2.5 Italia.