 SALUTE – Il fascino del prodotto griffato non risparmia nemmeno il settore farmaceutico, con conseguenze spesso non indifferenti per i nostri portafogli e per quelli del Sistema Sanitario Nazionale.
SALUTE – Il fascino del prodotto griffato non risparmia nemmeno il settore farmaceutico, con conseguenze spesso non indifferenti per i nostri portafogli e per quelli del Sistema Sanitario Nazionale.
Per favorire il mercato del farmaco generico equivalente, ancora scarso in Italia, Assogenerici ha dato il via a una campagna informativa che favorisca la scelta del farmaco non di marca rispetto al brand. Lo spot televisivo ha saputo cogliere l’ondata favorevole al generico avvallata dal recente decreto Monti sulle liberalizzazioni, che tuttavia lascia comunque in mano al medico sia la possibilità di informare dell’esistenza dell’equivalente, sia la facoltà di scegliere se aggiungere sulla ricetta la dicitura “non sostituibile”; in caso contrario spetta al farmacista distribuire la versione a prezzo inferiore a meno che non sia il paziente a richiedere la griffe, come spesso accade.
Il generico, da noi bistrattato, viene visto come meno efficace, a volte magari poco sicuro, diverso rispetto al suo parente famoso. In realtà per fregiarsi del titolo di farmaco equivalente è necessario ottenere l’approvazione da parte dell’Agenzia Italiana del Farmaco (AIFA) dimostrando la bioequivalenza rispetto al suo corrispettivo firmato.
Ma che cos’è esattamente un generico? Ogni anno scadono brevetti o vecchi Certificati Complementari di Protezione (CPC, estendono la protezione brevettuale al massimo di altri 18 anni), utilizzati per estendere la protezione del brevetto e ripagare l’azienda del tempo necessario tra il suo rilascio e la commercializzazione del farmaco, oggi sostituiti dal Supplementary Protection Certificate, che estende la protezione al massimo di altri 5 anni.
Queste scadenze possono aprire mercati importanti soprattutto quando la molecola è largamente consumata, permettendo un notevole risparmio ai cittadini e al Sistema Sanitario Nazionale.
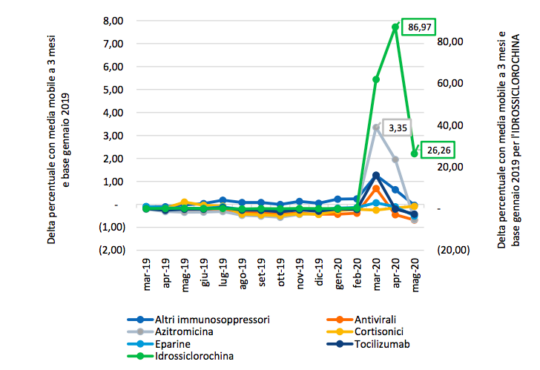
Il mercato dei generici ha infatti importanti margini di crescita. Un confronto tra i brevetti (o CPC) in scadenza in questi anni (fonte Assogenerici) con i princìpi attivi più consumati, tratti dal rapporto dell’Osservatorio sull’impiego dei medicinali (OsMed), mostra che vi sono certamente alcuni blockbuster “a rischio” di concorrenza non griffata, per esempio principi attivi appartenenti alla categoria dei farmaci contro l’ipercolesterolemia e gli antipertensivi.
Per capire quali siano i criteri scientifici previsti per legge che garantiscano l’equivalenza tra farmaci e i motivi dell’ancora forte diffidenza del pubblico, abbiamo intervistato Alberto Vaccheri, farmacologo e ricercatore all’Università di Bologna. “È la difficoltà nel distinguere parametri e variabilità permesse a generare problemi di fiducia”, spiega Vaccheri, “unita ad alcune difficoltà dell’informazione alle quali l’assessorato della Salute dell’Emilia Romagna sta cercando di porre rimedio, fissandosi come obiettivo principale la risalita del mercato del generico in Italia.”
Quali caratteristiche deve avere un farmaco generico per essere considerato equivalente al farmaco brand?
Un farmaco generico è un farmaco che può essere prodotto dopo la scadenza del brevetto, facendo perdere l’esclusiva a chi lo deteneva. Per essere considerato equivalente al cosiddetto originator (il brand), il farmaco deve mantenere la stessa identica quantità di principio attivo come previsto per legge. Può invece variare la sua biodisponibilità di più o meno 20% rispetto al farmaco brand e gli eccipienti.
Che cos’è la biodisponibilità?
La biodisponibilità è la percentuale di farmaco che si ritrova nel sangue dopo una somministrazione per via orale attraverso compresse, capsule. In caso il farmaco sia stato somministrato per via endovenosa questa concentrazione è del 100%.
Quindi possiamo definirla come la concentrazione plasmatica, ossia nel sangue, misurata dopo una somministrazione orale rispetto a quella che si misura dopo la somministrazione endovenosa.
Perché è accettabile questa variabilità di più o meno il 20% tra biodisponibilità del generico e del farmaco “griffato”?
Perché possiamo osservare la stessa variabilità all’interno dello stesso farmaco. Se somministrassimo l’originator a tante persone diverse oppure utilizzassimo diversi lotti su una stessa persona vedremmo una variabilità biologica che rispecchia quel 20% di tolleranza.
Con la vendita del generico non entra meno denaro a chi poi in realtà fa ricerca?
Il brevetto sui farmaci, che in Italia dura di più rispetto agli altri Paesi, esiste proprio per ripagare la ricerca, concetto a secondo me importante, purché gli investimenti ci siano.
L’abbassamento dei prezzi ha poco a che fare con la ricerca, perché non riguarda molecole nuove, che hanno prezzi molto più alti rispetto a quelli vecchi e della cui ricerca l’azienda verrà ripagata grazie al brevetto, ma di molecole vecchie delle quali alle aziende interessa poco dal punto di vista commerciale. Questo discorso vale soprattutto se parliamo di farmaci utilizzati anche dal medico di medicina generale che oggi rappresentano una piccola parte del mercato.
Il business si gioca invece su un altro campo, quello dei farmaci biologici, degli anticorpi monoclonali, dei farmaci antineoplastici, che hanno un ridotto numero di pazienti da trattare e prezzi altissimi. Quindi possiamo dire che i generici hanno sì innescato un circolo virtuoso sui prezzi dei farmaci laddove il loro uso si sia consolidato, favorendo un abbassamento dei prezzi di altre molecole analoghe e con le stesse indicazioni terapeutiche, ma protette ancora dal brevetto, senza però intaccare nuove molecole. Per questo sono uno strumento di contenimento della spesa e siccome la spesa per i farmaci è spesa pubblica, e la spesa pubblica ha risorse limitate, possiamo dire che contenere la spesa significa dare a tutti il più possibile.
Perché i medici non prescrivono volentieri questi generici?
Ci sono due credenze errate relative alla variabilità permessa per la biodisponibilità.
Molti pensano infatti che questo più o meno 20% di cui abbiamo parlato si riferisca al principio attivo, che ricordiamo è invece presente per legge in quantità identica rispetto a quella dell’originator.
Altra cosa è credere che questo 20% si riferisca alla sua attività, mentre come abbiamo visto si riferisce alla sua concentrazione nel sangue.
Com’è possibile che dei medici possano non avere queste informazioni?
Chi fa in Italia l’informazione ai medici? Per il 95% c’è l’industria e per il 5% c’è l’informazione pubblica. Quando Nello Martini era il direttore generale dell’AIFA, c’era un ufficio informazione e venivano mandati anche documenti ai medici. Nell’assetto attuale invece quel settore sta scomparendo e in più dobbiamo aggiungere che l’industria ha dei mezzi economici che il pubblico non possiede.