Lo smart patch per l’insulina, una svolta per il diabete
Niente iniezioni né il pericolo di sbagliare dosaggio: quando gli zuccheri nel sangue sono troppi il cerotto rilascia l'insulina, tarato sulle diverse necessità di ogni paziente
La parte difficile nel convivere con il diabete non sono le iniezioni di insulina, o il controllo della glicemia, o la dieta. È il fatto che devi fare tutte queste cose più volte al giorno, tutti i giorni per il resto della tua vita (John Buse, direttore del North Carolina Translational and Clinical Sciences Institute, ex presidente dell’American Diabetes Association)
SALUTE – Tre milioni di persone in Italia (il 4,9% della popolazione) sono malate di diabete, la malattia è stata loro diagnosticata e stanno seguendo un percorso terapeutico. Secondo i dati di Diabete Italia c’è poi un altro milione di persone che soffre di questa patologia ma che ancora non ha ricevuto una diagnosi. Un’ulteriore fetta intermedia, costituita da 2,6 milioni di persone, ha difficoltà nel mantenere le glicemie nella norma: si tratta di una condizione che nella maggior parte dei casi precede lo sviluppo del diabete di tipo 2.
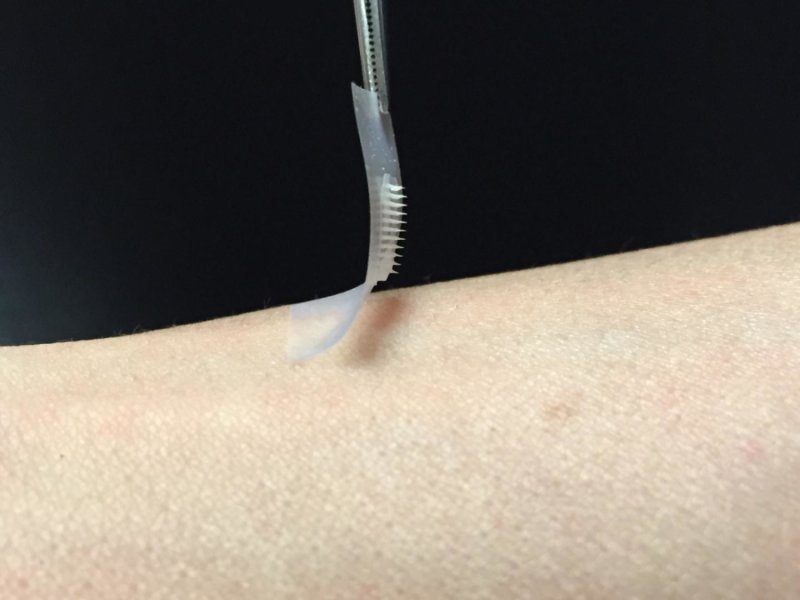
Ma un po’ come è successo per i vaccini sotto forma di cerotto (ne avevamo parlato qui) ora gli scienziati studiano un modo per lasciare nel passato le punture sul polpastrello e le dolorose iniezioni di insulina, e ne parlano su Proceedings of the National Academy of Sciences: si tratta di un patch, un cerotto “intelligente” che percepisce l’aumento dei livelli di zucchero nel sangue e, in base alla necessità, vi rilascia l’ormone. Niente siringhe e niente dolore. Lo smart patch è piccolo, quadrato e non più grande di una monetina: tutta la sua superficie è coperta da più di un centinaio di minuscoli aghetti, grandi come una ciglia e comprensivi di un’unità che contiene l’insulina ed enzimi che rilevano la concentrazione di glucosio. Si alzano i livelli nel sangue? Gli aghetti rilasciano il loro contenuto che entra subito in circolazione.
La ricerca ha verificato l’efficacia del cerotto su modelli murini per il diabete di tipo 1, lasciandolo applicato fino a nove ore di fila. I topi sono meno sensibili all’insulina rispetto agli esseri umani, e per questo gli scienziati pensano che l’effetto del patch potrebbe essere ben più longevo. L’ideale sarebbe riuscire a elaborare un cerotto che possa essere indossato senza mai toglierlo per vari giorni. Prima di passare a pazienti umani ovviamente ci vorrà del tempo, ulteriore ricerca pre clinica e poi finalmente i trial clinici. Ma le premesse sono incoraggianti, e fanno ben sperare quei 387 milioni di persone che in tutto il mondo soffrono di diabete. Un numero che si prevede non farà che aumentare negli anni, raggiungendo i 592 milioni di pazienti entro il 2035.
Gli altri punti di forza del patch sono la rapidità, la facilità con il quale si utilizza e i materiali: atossici e biocompatibili. Non è un caso che i ricercatori lo chiamino smart patch, visto che l’idea è modificarlo in base alle esigenze e alle caratteristiche di ogni singolo paziente, dal peso corporeo fino alla sensibilità all’ormone insulina. A differenza delle iniezioni, poi, il patch toglie il rischio dell’errore umano durante l’iniezione. “Iniettare la quantità sbagliata di medicinale può portare a complicazioni gravi come cecità e amputazione degli arti”, conferma John Buse dell’Università della North Carolina, co-autore senior della pubblicazione. “Nei casi peggiori si può arrivare al coma diabetico e alla morte”.
Per creare un “contenitore” adeguato per enzimi e insulina, i ricercatori hanno creato una nuova molecola partendo da acido ialuronico (una nota sostanza naturale presente in molti prodotti cosmetici) e dal 2-nitroimidazolo, un composto organico molto diffuso in diagnostica. La molecola è idrofilica a un’estremità e idrofobica dall’altra, ovvero da una parte lega con l’acqua e dall’altra ne viene respinta: questo permette di formare degli aggregati di molecole uniti in una vescicola, che gli scienziati paragonano alle gocce d’olio nell’acqua. La vescicola ospita gli enzimi che “monitorano” gli zuccheri nel sangue insieme all’insulina da iniettare.
Come viene rilasciato l’ormone nel sangue? All’aumento della glicemia il glucosio in eccesso si affolla nelle vescicole artificiali e viene convertito in acido gluconico dagli enzimi, consumando ossigeno durante il procedimento. A quel punto l’ipossia, ovvero la mancanza di ossigeno, fa diventare idrofiliche le molecole idrofobiche di 2-nitroimidazolo, la vescicola si disgrega e l’insulina raggiunge il sangue attraverso i capillari.
Va ricordato poi che a febbraio Sanofi ha lanciato sul mercato la sua insulina inalabile (se ne parlava da parecchio) perciò ora non resta che stare a vedere come si evolve la strada dei patch, che sembrano essere una delle nuove frontiere che si propongono di dire addio alle iniezioni. Che si tratti di vaccini oppure ormoni, semplificare il magazzinaggio, la distribuzione e la somministrazione non sarebbe già cosa da poco.
Leggi anche: Diabete e disturbi del comportamento, il ruolo dell’insulina
Pubblicato con licenza Creative Commons Attribuzione-Non opere derivate 2.5 Italia.
Crediti immagini: The lab of Zhen Gu, Ph.D.