Microscopia crioelettronica: il Nobel alla nuova era della biochimica
Il premio è stato assegnato a Jacques Dubochet, Joachim Frank e Richard Henderson che hanno progettato e sviluppato la microscopia crioelettronica, una tecnica che permette di studiare le biomolecole, ad esempio le proteine, in alta definizione con risoluzione atomica e preservando il campione
APPROFONDIMENTO – Congelare rapidamente il campione biologico e poi bombardarlo con un fascio di elettroni per vedere le strutture delle proteine nel minimo dettaglio senza danneggiarle. Questa è la tecnica della microscopia crioelettronica che è stata sviluppata negli ultimi 20 anni da Jacques Dubochet, Joachim Frank e Richard Henderson e che gli è valso l’ambito premio Nobel per la chimica 2017 assegnato dall’accademia svedese.
Un riconoscimento a un nuovo metodo per la visualizzazione delle biomolecole e che ha aperto alla biochimica la porta di una nuova era. Fino ad oggi infatti la tecnica, utilizzata con successo, era quella della cristallografia a raggi X, una tecnica che però presentava dei limiti, tra cui quello che non sempre le proteine formano un cristallo e il risultato non era quello sperato.
I tre scienziati hanno così cercato di superare quei limiti e sono riusciti a mettere a punto una tecnica che permette di avere una sorta di “fermo immagine” delle strutture complesse delle molecole biologiche, dando così la possibilità ai ricercatori di osservare e studiare questi biomolecole con una precisione senza precedenti e di esplorare la struttura tridimensionale di proteine come quelle che rendono i batteri resistenti agli antibiotici, oppure le proteine di superficie dei virus, come quella del virus Zika.
Nobel per la chimica: i vincitori

L’accademia svedese ha assegnato il premio ai tre scienziati congiuntamente. Dubochet, svizzero di 74 anni, ha studiato all’università di Ginevra e poi a Basilea e ora è professore onorario di Biofisica all’università di Losanna. Frank, tedesco di 77 anni, si è laureato al Politecnico di Monaco per poi trasferirsi negli Stati Uniti, dove ha insegnato Biochimica e biofisica molecolare nella Columbia University. Infine c’è Henderson, inglese di 72 anni, che dopo essersi laureato a Cambridge ha continuato a lavorare nel Laboratorio di Biologia molecolare del Medical Research Council (MRC) in Gran Bretagna.
Cos’è la microscopia crioelettronica?
La tecnica che è valsa il premio ai tre scienziati introduce il “freddo” in una tecnica che era già stata usata in precedenza. Il campione biologico viene vetrificato, cioè congelato rapidamente, in modo da essere immobilizzato senza venire danneggiato e poi essere bombardato di elettroni. Per lungo tempo infatti i microscopi elettronici sono stati ritenuti adatti solamente alla produzione di immagini di materia “morta”, perché i potenti fasci di elettroni sparati sul campione distruggono il materiale biologico.
I tre scienziati, in laboratori diversi, durante le loro ricerche erano stati chiamati a risolvere questo problema. Negli anni Novanta Henderson utilizzò il microscopio elettronico per generare immagini tridimensionali delle strutture delle proteine grazie anche ai risultati ottenuti da Frank tra il 1975 e il 1986, che dedicò i suoi esperimenti a rendere questa tecnica applicabile anche alla materia viva.
Ad aggiungere l’elemento acqua però è stato Dubochet: inserendo il liquido nella regione vuota del microscopio e facendolo solidificare velocemente, è riuscito a trovare il modo di imprigionare la biomolecola che si voleva osservare senza danneggiarla.
Anno dopo anno queste tecniche sono state affinate e il congelamento ha rappresentato il passaggio mancante per ottenere la preservazione della struttura biologica del campione, le cui immagini tridimensionali ora possono essere osservate e analizzate con una precisione di appena pochi Angstrom, cioè di un decimiliardesimo di metro. Una grandezza che ha portato lo studio delle immagini di biomolecole ad una risoluzione su scala atomica, come ha spiegato lo stesso Henderson dopo aver ricevuto il premio Nobel:
“Le prime strutture delle molecole biologiche sono state osservate con la cristallografia a raggi X nel 1959, con John Kendrew che ha vinto il Nobel per la Chimica lavorando sulle mioglobine e sviluppando il metodo a raggi X. Da allora abbiamo avuto centinaia, anzi migliaia di strutture studiate con questa tecnica, quindi in un certo senso la microscopia crioelettronica è solo un’altra tecnica per vedere qual è la struttura, su scala atomica e ad alta risoluzione, delle molecole. Ma la differenza è che ci sono alcune strutture in biologia che sono resistenti, come dire, recalcitranti agli altri metodi, come la cristallografia a raggi X o la spettroscopia a risonanza magnetica nucleare. Quindi si era creata la necessità di un nuovo metodo per approcciare a quell’area della struttura biologica che ci era ancora preclusa”.
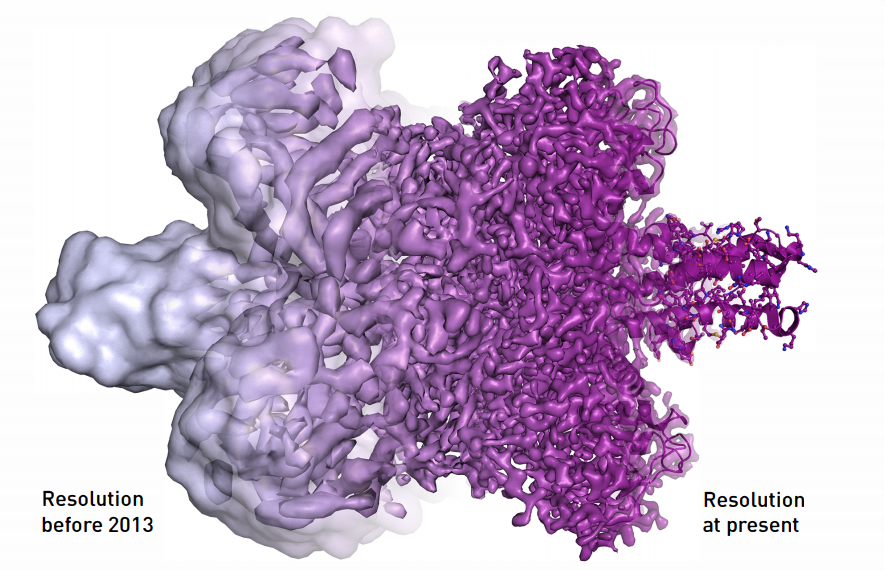
Una nuova era della biochimica
Le immagini, spiegano i ricercatori, sono alla base della biochimica. Fino ad oggi infatti nelle mappe biochimiche delle proteine c’erano dei “buchi”, cioè degli spazi vuoti che le immagini poco dettagliate non permettevano di identificare e riempire, come ha spiegato Henderson:
“Il mio primo lavoro è stato quello di studiare le proteine sulle membrane che trovavamo difficili da cristallizzare. Il vero potere di questo metodo però si osserva per quelle proteine che non hanno bisogno di essere cristallizzate, semplicemente le osserviamo, prendiamo i dati e li elaboriamo, al contrario della cristallografia che richiede di creare il cristallo, fare dei grafici di diffrazione e poi interpretarli. Penso che il nostro metodo sia diretto, un metodo facile da comprendere e che trova applicazione in moltissimi casi”.
Solo lo scorso anno, proprio la microscopia crioelettronica ha permesso di studiare nel dettaglio l’involucro del virus Zika, aprendo la strada alla progettazione di un possibile vaccino. Riuscire a vedere nel dettaglio le strutture di questi agenti patogeni, come anche i batteri resistenti agli antibiotici, permetterà infatti agli scienziati di disegnare e progettare farmaci che possano aderire perfettamente alle loro forme e neutralizzarli, aprendo una nuova era della biochimica e della farmaceutica.
Leggi anche: Nobel per la Chimica 2017 agli inventori della microscopia crioelettronica