4i, la tecnica innovativa per la medicina di precisione
La tecnica aumenta di 10 volte il numero di proteine visualizzate in un campione aprendo a nuovi orizzonti per le diagnosi e le prognosi dei pazienti oncologici
SCOPERTE – Visualizzare fino a 40 proteine in un unico campione di tessuto cellulare, un valore 10 volte maggiore di quelle attualmente visualizzate. Gli scienziati dell’università di Zurigo hanno messo a punto un nuovo metodo chiamato Iterative Indirect Immunofluorescence Imaging e chiamato appunto 4i che ha permesso di elevare gli standard dell’analisi cellulare ad un livello superiore in biomedicina. La tecnica 4i permette infatti di osservare la distribuzione spaziale di almeno 40 proteine, ma soprattutto di seguire le modificazioni che avvengono in una data cellula e per migliaia di cellule simultaneamente a vari livelli, tra tessuto e organi. Un modo di guardare ai campioni biologici decisamente nuovo e più completo, che ha applicazioni immediate anche nella medicina di precisione, come ad esempio negli studi sul cancro.
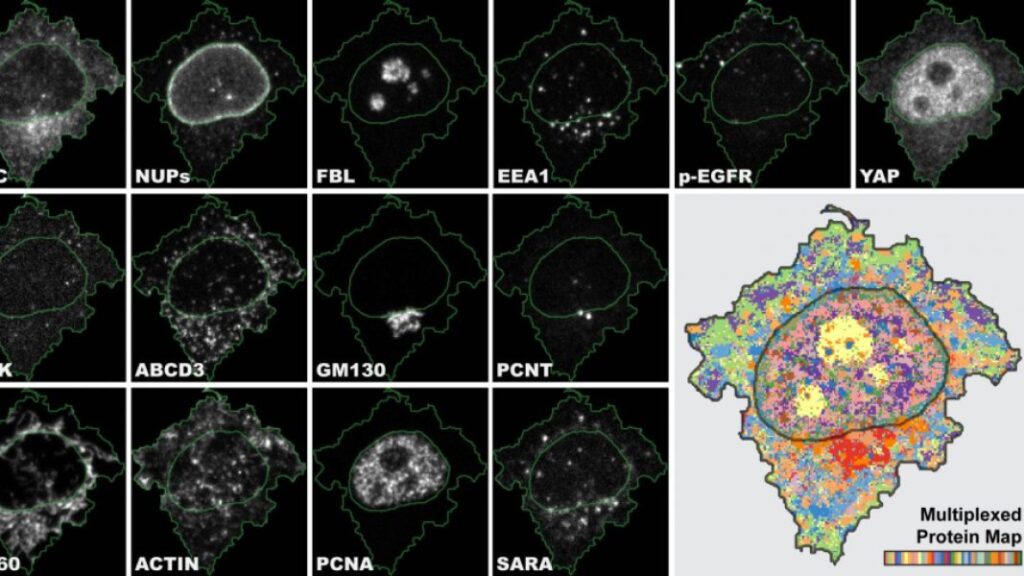
A sviluppare questa innovativa tecnica è stato il team di ricercatori guidati da Gabriele Gut, dell’Institute of Molecular Life Sciences a UZH, che ha pubblicato i risultati ottenuti sulla rivista Science e che spiega come la tecnica offra una vista multipla dei tessuti e permette di eseguire dei collegamenti fornendo così molteplici informazioni:
“4i è la prima tecnica di imaging che ci offre una vista dei campioni biologici dal semplice tessuto fino all’organo. Con questa tecnica possiamo collegare le molteplici informazioni che ricaviamo dai campioni sia a livello cellulare che subcellulare in un unico esperimento”.
Differenze tra le tecniche tradizionali e la 4i
Ad oggi la tecnica più utilizzata è quella dell’immunofluorescenza (IF) in cui si utilizzano gli anticorpi per visualizzare e localizzare le proteine nei campioni biologici. Nella IF standard le proteine vengono marcata, mentre 4i utilizza gli anticorpi e la fluorescenza microscopica convenzionale per visualizzare 10 volte più proteine reiterando l’ibridizzazione e la rimozione degli anticorpi dal campione stesso. Gut ha spiegato:
“Immaginate che i biologi cellulari siano dei giornalisti. Ogni esperimento è una intervista con le nostre cellule. Con la IF convenzionale possiamo fare solo tre domande all’intervistato, mentre con 4i possiamo intraprendere una discussione su oltre 40 argomenti”.
Il risultato è una mappa realizzata con una grande quantità di dati, che richiede però anche un sistema per poterli analizzare. Il metodo, infatti, permette di generare immagini con risoluzione subcellulare per migliaia di cellule, con 40 canali e oltre 10 condizioni di trattamento. Una quantità di informazioni che genera una complessità biologica impossibile da processare dal solo occhio umano e dal cervello.
Proprio per poter sfruttare al meglio i dati raccolti con 4i è stato necessario sviluppare anche un software per la visualizzazione e l’analisi dei dati che i ricercatori hanno chiamato Multiplexed Protein Maps. Il programma è così in grado di estrarre i molteplici segnali fluorescenti che valgono milioni di pixel e generare una mappa rappresentativa e riassuntiva della distribuzione delle proteine nelle cellule.
La mappa così ottenuta permette di generare una rilevazione sistematica dello scenario cellulare, consentendo di visualizzare l’organizzazione spaziale intracellulare della maggior parte degli organelli lungo tutto il ciclo cellulare e in differenti microambienti. Questa tecnica rappresenta dunque una importante innovazione nella biomedicina, soprattutto per le sue potenziali applicazioni dalla ricerca di base fino alla medicina di precisione. Gut ha spiegato:
“Speriamo che 4i e multiplexed protein maps aiuteranno i ricercatori a comprendere a meglio i processi che sono al centro della ricerca biologica da decenni”.
A cosa può servire questa tecnica?
La tecnica infatti può essere utilizzata per determinare gli effetti delle sostanze farmacologiche sulla organizzazione e fisiologia delle cellule, tanto che al momento 4i viene impiegata in una collaborazione di ricerca con medici e casa farmaceutiche proprio con l’obiettivo di migliorare la risposta farmacologica dei pazienti tumorali. Lucas Pelkmans, professore dell’Institute of Molecular Life Science di Zurigo e il suo team stanno cercando di caratterizzare le cellule tumorali dei pazienti che sono stati trattati con diverse terapie farmacologiche, con lo scopo di ottenere risultati in laboratorio che permettano di orientare la scelta della terapia affinché sia quella più adatta al singolo paziente. Un risultato importante per una tecnica che è solo agli inizi, dato che il prossimo passo dei ricercatori sarà quello di implementare sia 4i che il sistema di analisi sulle sezione di tessuti tumorali per identificare biomarcatori importanti e ottenere migliori diagnosi e prognosi per i pazienti oncologici.
Segui Veronica Nicosia su Twitter
Leggi anche: Le neuroscienze cognitive incontrano le intelligenze artificiali
Pubblicato con licenza Creative Commons Attribuzione-Non opere derivate 2.5 Italia. 





