Proteine in 3D: dimmi con che amminoacido vai e ti dirò come sei
Per risolvere il problema del ripiegamento delle proteine, i modelli biofisici più recenti considerano non tanto le singole sequenze di amminoacidi quanto insiemi di sequenze diverse che hanno struttura e funzione simile in specie diverse
Le proteine sono i principali attori di tutto ciò che succede nella cellula e dal loro corretto funzionamento dipende la vita di un organismo. Il loro studio è importante anche in campo medico perché molte delle malattie esistenti sono dovute a qualche errore a livello proteico. Tuttavia, molti dei meccanismi, interazioni, strutture che coinvolgono le proteine restano ancora con un punto di domanda.
Edoardo Sarti è alla Sorbonne di Parigi per studiare la struttura di proteine e di complessi proteici a partire dall’informazione contenuta nella sequenza di amminoacidi, dalla loro somiglianza e dalla loro conservazione nel corso dell’evoluzione.
Nome: Edoardo Sarti
Età: 32 anni
Nato a: Milano
Vivo a: Parigi (Francia)
Dottorato in: biofisica e fisica statistica (Trieste)
Ricerca: Determinare l’interazione tra proteine attraverso segnali coevolutivi
Istituto: Statistical Genomics and Biological Physics, Laboratory of Computational and Quantitative Biology (LCQB) Sorbonne Université (Parigi)
Interessi: leggere, giochi da tavola e di ruolo, studiare filosofia della scienza,
Di Parigi mi piace: la multiculturalità, la densità di cultura
Di Parigi non mi piace: il sistema degli affitti, il costo degli immobili
Pensiero: Considerate la vostra semenza: fatti non foste a viver come bruti, ma per seguir virtute e canoscenza. (Dante Alighieri)
Il comportamento di molte proteine è ancora sconosciuto. Quali sono le difficoltà in questo campo?
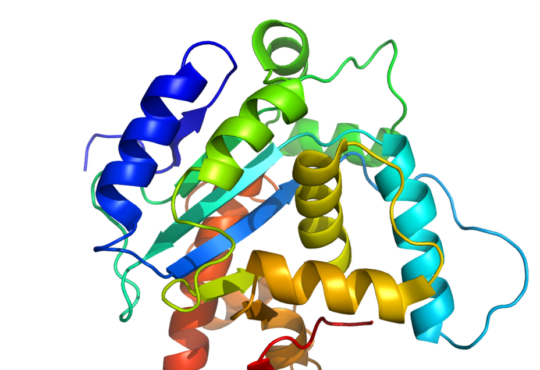
Per studiare la funzione di una proteina di solito si ricorre a due tipi di esperimenti: il primo riguarda la struttura primaria, cioè la sequenza di amminoacidi che la compongono. Diverse combinazioni di amminoacidi portano a diversi ripiegamenti e forme della proteina e a diverse funzioni.
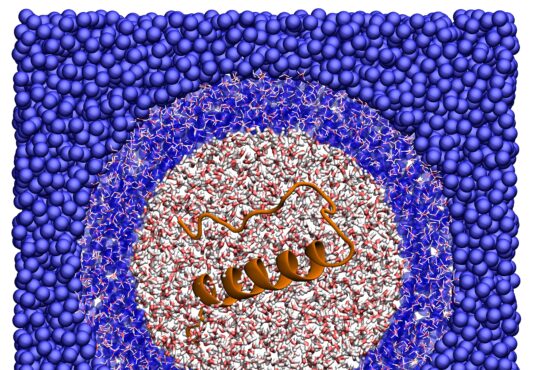
Il secondo tipo di approccio riguarda la struttura tridimensionale di queste molecole: sapendo come si dispongono nello spazio e se magari venisse fuori che alcune si ripiegano in modo simile a proteine già caratterizzate, potremmo fare delle ipotesi più verosimili sulla loro funzione.
Purtroppo gli esperimenti sulla struttura 3D delle proteine sono ancora molto costosi, ci vogliono anni e anni e, per le tecniche più accurate, si procede praticamente al buio fino a quando si trova la giusta combinazione di reagenti con cui evidenziare una struttura.
Esistono approcci alternativi agli esperimenti?
Attualmente il metodo che va per la maggiore è quello delle reti neurali. Ci sono algoritmi che riescono a predire in maniera spesso corretta la struttura di certe proteine, ne abbiamo conferma in laboratorio; purtroppo non possiamo sapere come fanno a rielaborare i dati per arrivare alla risposta giusta. Quindi è effettivamente un approccio utilissimo per conoscere come è fatta la tal proteina, ma se vogliamo sapere perché ha quella forma o perché interagisce in quella maniera, le reti neurali non ci sono di nessun aiuto.
Nel mio laboratorio usiamo un approccio diverso, basato su modelli statistici inventati a inizio Novecento per studiare tutt’altro, che sfrutta l’informazione presente non solo nella sequenza della proteina di interesse ma anche in quella di proteine appartenenti alla stessa famiglia e quindi a essa evolutivamente e funzionalmente somiglianti.
Infatti, esistono proteine che si sono conservate nel corso dell’evoluzione e che ritroviamo con la stessa funzione anche in specie molto lontane tra loro; certo, una distanza evolutiva c’è, non è che la sequenza di amminoacidi sia rimasta immutata, ma è vero che per certi meccanismi cellulari non siamo poi così distanti dai pesci rossi.
Cosa cercate in queste sequenze?
Vediamo cosa cambia e cosa rimane uguale tra le varie proteine, a livello di regioni che si assomigliano.
Se nel corso dell’evoluzione un amminoacido è rimasto sempre nella stessa posizione e non è cambiato dal lievito al pesce rosso fino a noi, allora vuol dire che quell’amminoacido è molto importante. E possiamo valutare il perché si sia conservato.
Un’altra considerazione che si può fare è: se vediamo due amminoacidi che cambiano e lo fanno sempre nello stesso momento, può voler dire che una mutazione a carico del primo ha in qualche modo costretto il secondo a fare lo stesso, per sopravvivere, per far funzionare la proteina. Si parla di coevoluzione. Inoltre, è probabile che i due amminoacidi siano in qualche modo a contatto o comunque vicini l’uno all’altro perciò, facendo una lista di tutte le coppie di amminoacidi che cambiano assieme, possiamo ricavare buoni indizi sulla struttura della proteina.
Attenzione, non è detto che ogni volta che due residui cambiano nello stesso momento allora sono vicini. Pensiamo a tre residui a contatto l’uno con l’altro: il primo cambia e, per coevoluzione, cambia anche il secondo. Anche il terzo potrebbe cominciare a cambiare, sotto la spinta dell’evoluzione del secondo, quindi è vero che vedo cambiare assieme 1 e 2, ma anche 2 e 3 e, soprattutto, 1 e 3, che non sono affatto vicini!
Come si possono distinguere le coppie vicine da quelle che non lo sono?
Il mio capo ha inventato un metodo statistico proprio per pulire il segnale di correlazione delle pseudo coppie che cambiano assieme ma non sono vicine nella struttura. Si chiama DCA (Direct Coupling Analysis) ed è un metodo di inferenza sull’informazione contenuta nelle sequenze. Il tutto si basa su modelli fisici come quello di Ising e di Potts.
In questi modelli c’è un reticolo di oggetti che possono trovarsi in varie configurazioni e la cui interazione può essere descritta da una funzione energia che dipende dalla direzione in cui questi si trovano. Nel nostro caso, le direzioni sono i vari tipi di amminoacido. In base alle statistiche di mutazione di singoli/coppie di amminoacidi e sapendo se ricandono dentro la funzione energia o no, possiamo stabilire se due oggetti stanno effettivamente vicini.
Il modello DCA non dà, quindi, la struttura della proteina ma una serie di probabilità e correlazioni.
Quali sono le prospettive future del tuo lavoro?
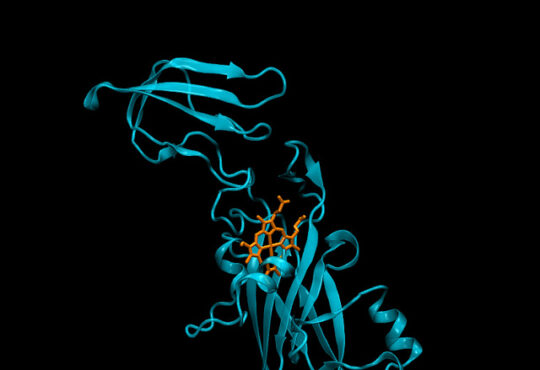
Vorrei usare il DCA per determinare la struttura di complessi di molecole e risolvere il problema delle interazioni proteina-proteina.
Inoltre, voglio continuare a testare i modelli DCA che sviluppiamo su proteine di struttura nota. E, in futuro, mi piacerebbe combinare la mia pregressa conoscenza delle proteine di membrana con i metodi DCA per aumentare la loro precisione anche in casi particolari come questi.
Leggi anche: La rivoluzione delle strutture proteiche 3D
Pubblicato con licenza Creative Commons Attribuzione-Non opere derivate 2.5 Italia. ![]()
Immagine copertina: Pixabay