Dalla scrapie al morbo Creutzfeldt-Jakob per svelare i misteri dei prioni
I ricercatori dell'Istituto Superiore di Sanità hanno identificato un prione incapace di riprodursi in vivo, ma che continua a farlo in vitro. È l'ultima di una serie di scoperte che ci avvicinano a capire meglio queste proteine "difettose"

SCOPERTE – Gli scienziati dell’Istituto Superiore di Sanità di Roma, guidati da Ilaria Vanni, sono riusciti per la prima volta a isolare un prione mutante, che non è in grado di moltiplicarsi negli animali ma solamente in laboratorio, dunque in provetta: si tratta di un passo importante per capire nel dettaglio come funziona il meccanismo infettivo di queste proteine “difettose”. I risultati dello studio sono stati pubblicati su Plos Pathogens.
Il lavoro di Vanni e colleghi si è concentrato su un’encefalopatia trasmissibile chiamata scrapie, che dopo un’incubazione anche molto lunga (dai pochi mesi agli anni) colpisce il sistema nervoso degli ovini, pecore e capre, portandoli a un’andatura barcollante. Gli animali affetti dalla malattia perdono la lana a zone, sono colpiti da alopecia e possono avere comportamenti particolari, diventando per esempio insolitamente aggressivi o molto paurosi. Ma soprattutto iniziano a grattarsi con insistenza fino a provocarsi ferite, da cui il nome scrapie, dal verbo inglese to scrape: grattare, graffiare.
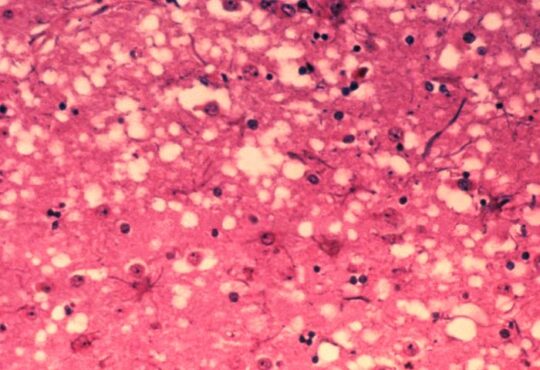
A causare questa malattia degenerativa, un’encefalopatia spongiforme – così chiamata per l’aspetto che assume il cervello colpito – è un prione. Si tratta di una proteina “corrotta”, che per motivi ignoti sfugge ai normali meccanismi di demolizione dell’organismo. I prioni rimangono all’interno della cellula nonostante la loro forma anomala e iniziano a convertire alla stessa forma anche le proteine sane, che abbandonano la loro attività consueta e si comportano come il prione. Quando molti di questi prioni si accumulano nelle cellule del sistema nervoso, per esempio nei mammiferi come bovini e ovini, ne compromettono il funzionamento e causano diverse patologie come la BSE, più nota come sindrome o morbo della mucca pazza, i cui primi casi risalgono a circa trent’anni fa, in Gran Bretagna.
Negli esseri umani i prioni causano invece il morbo di Creutzfeldt-Jakob, una rara malattia neurodegenerativa identificata intorno al 1920 e che conduce alla morte chi ne è colpito, ma anche l’insonnia fatale familiare: colpisce pochissime persone nel mondo e si origina dalla stessa mutazione del Creutzfeldt-Jakob, in un sito genico diverso. Il nome parla chiaro: chi ne soffre non riesce più a dormire, e la deprivazione finisce per condurre alla morte.
Precedenti ricerche avevano già scoperto che, in particolari condizioni, la conformazione di un prione può mutare. I ricercatori guidati da Vanni hanno continuato a lavorare in quella direzione e hanno scoperto che tra le varie conformazioni dei prioni presenti in natura ne esiste una che continua sì a riprodursi in laboratorio (una capacità che tutti i prioni mantengono) ma non riesce più a farlo in un organismo vivente. Quando hanno inserito questi prioni mutati in un gruppo di arvicole, dei piccoli roditori, è arrivata la conferma: nessuno degli animali si è ammalato.
L’unica differenza tra il prione mutato e quello non mutato è la mancanza di una serie di aminoacidi, che potrebbe rivelarsi la chiave della capacità di un prione di causare l’infezione e la conseguente patologia. Allo stesso tempo, l’alterazione non impedisce a queste proteine mortali di continuare a moltiplicarsi in vitro. Ora Vanni e colleghi continueranno a lavorare con il prione mutato, per studiare come “si evolve” in provetta la popolazione che hanno derivato dalle pecore malate di scrapie. Il fatto che queste conformazioni incapaci di replicarsi in vivo esistano è già un ottimo indizio della direzione da seguire per capire come una proteina mal-ripiegata si trasformi in un prione mortale. Prima di diventare il temibile prione, infatti, la proteina prionica (PrPc) ha un’importante funzione neuroprotettiva. In che modo agisse è rimasto a lungo poco compreso, fino a quando una serie di studi, qualche anno fa, ha iniziato gradualmente a svelare il meccanismo molecolare con cui protegge i nostri neuroni.
Nel 2015 il gruppo di ricerca guidato da Giuseppe Legname, alla SISSA di Trieste (Laboratory of Prion Biology), l’ha descritto in uno studio pubblicato sulla rivista Antioxidants and Redox Signaling: la proteina prionica modula il meccanismo di apertura e chiusura dei canali che permettono il passaggio di ioni calcio all’interno del neurone, fondamentali nella trasmissione dei segnali nervosi. Una volta che il canale è aperto la PrPc ne consente una rapida chiusura, in modo che nella cellula non entrino troppi ioni calcio: potrebbero causarne la morte. Quando è ripiegata male, diventando prione, questa funzione non può più essere svolta correttamente. Lo stesso gruppo, collaborando con l’istituto BESTA di Milano, ha sintetizzato prioni artificiali, più facili da controllare ed estremamente utili per studiare i meccanismi che potrebbero bloccare l’effetto patogeno. A marzo 2015 un’altra importante novità: un gruppo di ricerca milanese ha sviluppato il primo modello murino per studiare l’insonnia fatale familiare, della quale sappiamo ancora pochissimo nonostante sia stata descritta oltre trent’anni fa.
Inoltre, quest’estate Nature Reviews Neurology ha pubblicato un articolo, a firma di un gruppo di ricercatori italiani e americani, in cui si descrive un test innovativo per la diagnosi precoce della malattia di Creutzfeldt-Jakob ancora prima che compaiano i sintomi. Il primo autore della review, Gianluigi Zanusso del dipartimento di Neuroscienze dell’università di Verona, è stato premiato per il miglior studio di diagnostica umana al congresso mondiale Prion 2016. “Poiché molte malattie neurodegenerative possono mimare il morbo di Creutzfeldt-Jakob, avere la certezza che lo sia oppure no permette di fare un’altra diagnosi, di cercare un’altra causa e, quindi, una potenziale terapia”, ha raccontato Zanusso in un’intervista a Wired Italia. “Perché la realtà non è cambiata: nel momento in cui si fa una diagnosi di Cjd si emette una sentenza di morte, non c’è nessun tipo di terapia che possa fare qualcosa”.
Leggi anche: L’Alzheimer si può trasmettere?
Pubblicato con licenza Creative Commons Attribuzione-Non opere derivate 2.5 Italia. ![]()