Trascrittomi spaziali e tessuti vegetali
Grazie a una particolare tecnica è possibile analizzare specifiche sezioni di un tessuto, con una precisione mai raggiunta prima.
SCOPERTE – Nel luglio del 2016 un gruppo internazionale di ricercatori dello Science for Life Laboratory, (SciLifeLab), realtà svedese di ricerca biomolecolare, ha pubblicato su Science i risultati di uno studio volto a presentare una nuova e più efficace tecnica per l’analisi istologica dei tessuti animali. Il gruppo, coordinato dai biotecnologi Patrik L. Ståhl, Fredrik Salmén e Joakim Lundeberg, ha ideato un metodo, denominato trascrittomi spaziali, che permette di giungere a un’analisi visiva e quantitativa del trascrittoma – l’insieme dei trascritti (mRNA) di un organismo – delle singole sezioni di un tessuto. I benefici nella ricerca e nelle diagnosi sono innegabili: i trascrittomi spaziali rendono possibile l’indagine istologica su specifiche sezioni di un tessuto, con una precisione mai raggiunta prima.
Recentemente un gruppo di ricerca coordinato da Stefania Giacomello, biotecnologa del SciLifeLab che aveva contribuito allo sviluppo della nuova tecnologia, ha rivisitato la tecnica e ha dimostrato come sia possibile applicarla anche per lo studio dei tessuti vegetali. I dettagli della nuova scoperta sono stati pubblicati a maggio su Nature plants.
Perché è stato necessario un nuovo studio per verificare l’efficacia della tecnica sui vegetali? “Sia le cellule degli animali che quelle delle piante possiedono una membrana”, ha spiegato la dottoressa Giacomello, “solo che queste ultime hanno anche una parete che conferisce una certa rigidità ai tessuti; basta pensare alla robusta consistenza del legno, frutto delle strutture intercellulari che lo caratterizzano. L’efficacia del nuovo metodo su questi tessuti non era così scontata”.
La tecnica dei trascrittomi spaziali si basa su una modifica, mai sostanziale come in questo caso, dei comuni vetrini da microscopio. “Sulla superficie del vetrino ci sono sei quadrati, chiamati array, che in italiano potremmo denominare ‘matrici’. Ogni matrice è suddivisa in 1007 piccole celle circolari che contengono circa 200 milioni di sonde. Esse sono le stesse per ognuna delle celle ma sono contraddistinte da una importante differenza: un codice a barre che ne identifica l’esatta posizione, come una propria personale carta d’identità”, illustra la ricercatrice, che chiarisce come l’intero processo preveda una serie di passaggi minuziosi per giungere a un risultato utile e soddisfacente.
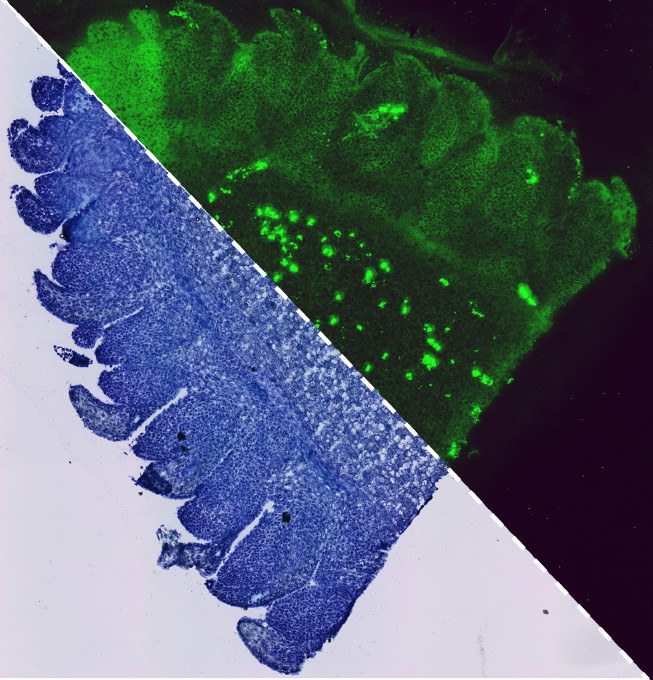
“Per prima cosa otteniamo una ‘foto’ del tessuto. Una volta posizionato sul vetrino il tessuto d’interesse, sia esso di un mammifero o di una pianta, viene fatto un processo di imaging applicando reagenti chimici per fissare la morfologia del tessuto senza che ci sia il rischio di un’alterazione nel tempo. Una volta fatto questo, si passa alle reazioni di permeabilizzazione grazie alle quali apriamo le cellule e facciamo fuoriuscire l’mRNA. I trascritti scendono verticalmente e vengono catturati dai sensori”.
Non si tratta di un’operazione semplice. Il rischio è quello di aprire troppo le cellule, sparpagliando i loro trascritti sulla superficie al punto da perdere la risoluzione spaziale e la capacità di essere precisi.
“Per scongiurare questo rischio e per capire se questo passo è stato compiuto a dovere utilizziamo il fluorescent cDNA, un’impronta fluorescente dei trascritti dell’mRNA del tessuto in esame. I sensori, infatti, funzionano come uno stampo grazie a cui possiamo ottenere, in un intervallo di tempo di circa una notte, le copie di cDNA. Il giorno successivo rimuoviamo in laboratorio il tessuto e attraverso adeguati microscopi visualizziamo l’impronta fluorescente. Se le condizioni di permeabilizzazione risultano opportune, ripetiamo l’esperimento producendo le copie di cDNA senza fluorescenza e il giorno successivo raccogliamo, grazie ad alcune reazioni enzimatiche, i sensori del vetrino. Essi vengono sottoposti a un processo chiamato ‘di amplificazione’, un modo per ottenere più copie, necessarie nel momento in cui, durante il sequenziamento, è fondamentale avere una sorta di massa critica per ottenere dati validi”.
Una volta eseguito il sequenziamento – il processo con cui ottenere tutte le informazioni genetiche insite nelle sequenze di DNA – i trascritti vengono confrontati con il genoma di riferimento.
“In questo modo è possibile vedere quante copie di un dato trascritto erano espresse e dove. Si tratta di un processo bioinformatico dato che, alla fine, si ottiene una matrice computazionale. A questo punto è possibile combinare questa informazione bioinformatica con le immagini raccolte all’inizio: le sovrapponiamo, per così dire, e riusciamo a vedere dove esattamente i trascritti erano espressi nel tessuto”.
Grazie al lavoro compiuto dalla dottoressa Giacomello e dai suoi colleghi i trascrittomi spaziali potranno essere applicati in nuovi campi di studio.
“Uno dei campi di applicabilità nell’immediato è quello dell’agricoltura. Per esempio è possibile studiare i geni che controllano la quantità di semi che una pianta genera per migliorarne e accelerarne la produzione. Questa tecnologia identifica qualsiasi gene codificato nel genoma e ha un target completo, non ne studia uno alla volta. Permette di eseguire una serie intera di studi di base per sviluppare nuove applicazioni in futuro. Si può applicare a sistemi quantitativi oppure è possibile indagare i sistemi di differenziamento cellulare nelle piante. Sono convinta che la nostra tecnica possa essere utilizzata in una grande varietà di campi di ricerca”.
Leggi anche: Una nuova tecnica di microscopia infrange la “barriera del colore”
Pubblicato con licenza Creative Commons Attribuzione-Non opere derivate 2.5 Italia. ![]()





