Studio rivela: l’epigenetica influenza davvero i nostri discendenti
Uno studio ha scoperto che, nella riproduzione, le informazioni epigenetiche non solo vengono ereditate da una generazione all'altra, ma anche che sono importanti per lo sviluppo dell'embrione.
SCOPERTE – Epigenetica: un termine nel quale non è difficile imbattersi negli ultimi tempi. Ma cosa significa? Come sappiamo, ognuno di noi eredita 23 cromosomi dalla madre e altrettanti dal padre, e questi cromosomi vanno a costituire il nostro patrimonio genetico (o genoma). Però ciò che siamo non è determinato solo dal genotipo: l’insieme dei nostri tratti fisici, il fenotipo, dipende da come i geni interagiscono con l’ambiente. Ed è qui che entra in gioco l’epigenetica ovvero tutte le modifiche chimiche a carico di DNA o regioni vicine che variano l’espressione genica, pur non alterando la sequenza dei nucleotidi. Più semplicemente, quei cambiamenti che influenzano il fenotipo senza alterare il genotipo.
Tali cambiamenti contrassegnano regioni specifiche del DNA in modo da attirare o tenere a distanza le proteine che attivano i geni. Contrariamente alla sequenza fissa di basi azotate (A T C G) nel DNA, i contrassegni epigenetici possono anche cambiare per tutta la vita e in risposta ad ambiente, stile di vita, malattia o dieta, e si suppone che restino conservati nella memoria epigenetica delle cellule. A lungo ci si è chiesto se possano attraversare il confine delle generazioni ed essere ereditate dai figli o addirittura dai nipoti.
Pubblicata su Science, la risposta giunge da uno studio del dipartimento di Immunobiologia ed Epigenetica dell’Istituto Max Planck di Friburgo, che porta solide prove sia sulla regolazione dell’espressione genica nella prole che sullo sviluppo e la sopravvivenza della nuova generazione. Si credeva che la memoria epigenetica accumulatasi nel corso di una vita venisse completamente eliminata durante lo sviluppo di spermatozoi e cellule uovo, ma solo di recente alcuni studi hanno dimostrato che i segni epigenetici possono essere trasmessi per generazioni (ma come e con quali effetti sulla prole, non è ancora chiaro).
“Abbiamo visto segni di eredità intergenerazionale di informazioni epigenetiche a partire dalla nascita dell’epigenetica nei primi anni Novanta. Ad esempio, gli studi epidemiologici hanno rivelato una lampante correlazione tra l’offerta di cibo dei nonni e un aumento del rischio di diabete e malattie cardiovascolari nei loro nipoti.” dice Nicola Iovino, uno degli autori dello studio. “Da allora, diversi rapporti hanno fatto pensare a eredità epigenetica in organismi diversi, ma i meccanismi molecolari erano sconosciuti”.
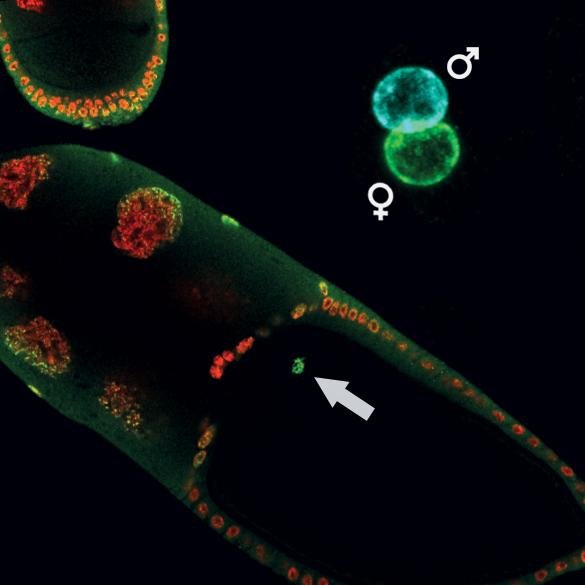
Il ricercatore e il suo gruppo hanno operato sulle mosche della frutta, concentrandosi su una modifica chiamata H3K27me3, presente anche negli esseri umani. Questa altera la cromatina (che racchiude il DNA nel nucleo della cellula) ed è principalmente associata alla repressione dell’espressione genica. I ricercatori hanno scoperto che le modificazioni di H3K27me3 nelle cellule uovo della madre erano ancora presenti nell’embrione dopo la fecondazione, anche se altri marchi epigenetici erano stati cancellati.
“Questo indica che la madre passa i suoi marchi epigenetici alla prole. Ma ci interessava anche se questi marchi stessero facendo qualcosa di importante nell’embrione” spiega Fides Zenk, primo autore dello studio. Gli scienziati hanno quindi utilizzato diversi strumenti genetici per rimuovere l’enzima che marca H3K27me3 e hanno scoperto che gli embrioni privi di H3K27me3 durante lo sviluppo iniziale non potrebbero svilupparsi fino alla fine dell’embriogenesi.
“Si è scoperto che, nella riproduzione, le informazioni epigenetiche non solo vengono ereditate da una generazione all’altra, ma anche che sono importanti per lo sviluppo dell’embrione stesso”, aggiunge Iovino. Quando la squadra ha esaminato più da vicino gli embrioni, si è resa conto che alcuni importanti geni regolatori dello sviluppo, normalmente spenti durante la prima embriogenesi, erano stati accesi in embrioni senza H3K27me3.
“Abbiamo supposto che attivare questi geni troppo presto durante lo sviluppo abbia interrotto l’embriogenesi e infine abbia causato la morte dell’embrione”, illustra Zenk. “Sembra, in pratica, che siano necessarie informazioni epigenetiche ereditarie per elaborare e trascrivere correttamente il codice genetico dell’embrione”.
“Il nostro studio indica che ereditiamo più che i soli geni dei nostri genitori. Sembra che abbiamo anche un’importante e raffinato meccanismo di regolazione, che può essere influenzato dal nostro ambiente e dal nostro stile di vita. Queste conoscenze possono fornire nuove basi per osservare che almeno in alcuni casi gli adattamenti ambientali acquisiti possano essere passati sulla linea germinale alla nostra discendenza” conclude Iovino.
Questi nuovi risultati potrebbero avere implicazioni per la salute umana, poiché l’interruzione dei meccanismi epigenetici può causare malattie come cancro, diabete e disturbi autoimmuni.
Segui Giovanni De Benedictis su Twitter
Leggi anche: Epigenetica e uccelli: un’evoluzione verso l’intelligenza?
Pubblicato con licenza Creative Commons Attribuzione-Non opere derivate 2.5 Italia. ![]()