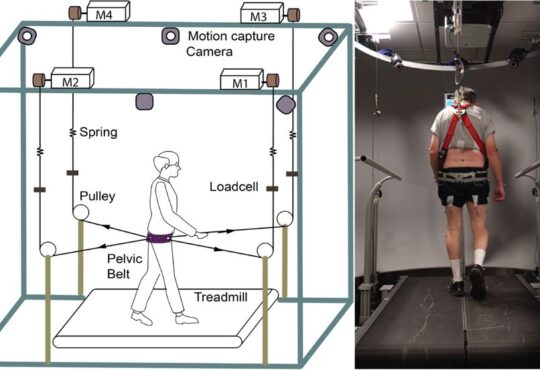
Malattia di Huntington: il ruolo delle cellule gliali
I disturbi cognitivi della patologia sono associati alla degenerazione della sostanza bianca del cervello. La causa sembra essere il mancato sviluppo delle cellule gliali che avvolgono i neuroni.
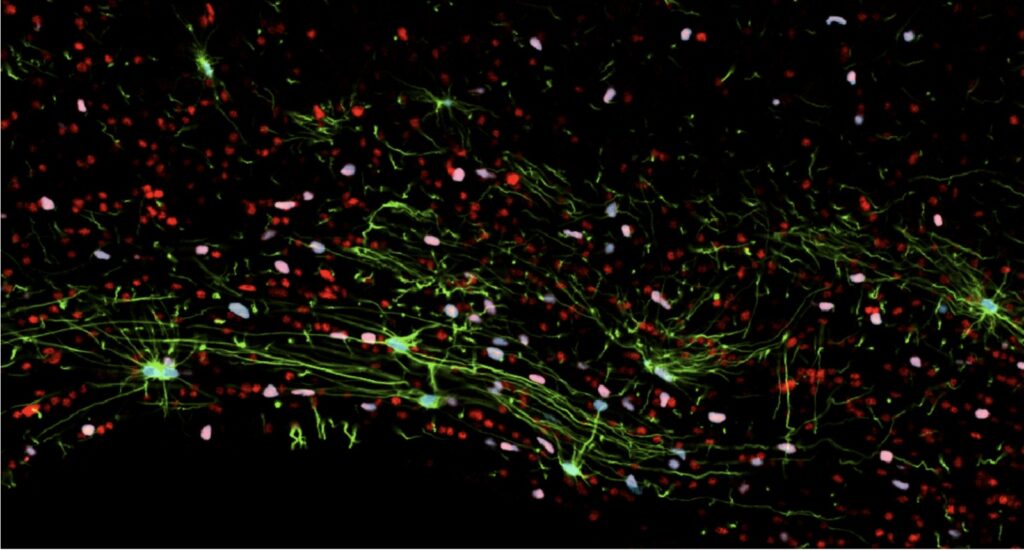
RICERCANDO ALL’ESTERO – La malattia di Huntington è una malattia neurodegenerativa caratterizzata da una lenta e progressiva perdita del controllo muscolare, disturbi cognitivi e alterazioni della personalità e dell’umore. È causata da una mutazione nel gene della huntingtina per cui la proteina mutata si accumula nel cervello e danneggia le cellule nervose, in particolare i neuroni spinosi medi.
Rossana Foti è una ricercatrice del Center for Translational Neuromedicine di Copenhagen e si occupa della patogenesi della malattia di Huntington. Studia il coinvolgimento delle cellule gliali, le cellule che supportano i neuroni e li ricoprono di una guaina mielinica che permette di trasmettere l’impulso nervoso più velocemente.
 Nome: Rossana Foti
Nome: Rossana Foti
Età: 38 anni
Nata a: Siracusa
Vivo a: Copenhagen (Danimarca)
Dottorato: genomica funzionale e strutturale (Trieste)
Ricerca: Epigenomica di cellule precursori di oligodendrociti derivate dalla malattia di Huntington
Istituto: Center for Translational Neuromedicine, University of Copenhagen (Danimarca)
Interessi: viaggiare, giocare con mio figlio, andare in bicicletta
Di Copenhagen mi piace: è tutto orientato ai bambini, il verde, il mare, si può tranquillamente girare in bicicletta, c’è molta attenzione all’equilibrio vita-lavoro
Di Copenhagen non mi piace: la mancanza di luce è deprimente, il cibo
Pensiero: La verità si ritrova sempre nella semplicità, e non nella complessità e confusione delle cose. (Isaac Newton)
Cosa succede alle cellule gliali nei pazienti affetti dalla malattia di Huntington?
Si è visto che queste cellule cominciano a scomparire diversi anni prima che i pazienti mostrino i sintomi motori tipici della malattia, cioè movimenti scoordinati che diventano involontari e casuali per poi scomparire del tutto. Fino a 10 anni prima della comparsa dei sintomi motori, si possono manifestare deficit cognitivi e alterazioni della personalità: con una risonanza magnetica si può vedere che tali disturbi sono associati a perdita di sostanza bianca nel cervello. Con la mia ricerca vorrei trovare la causa della di questa perdita; l’ipotesi che stiamo verificando è che sia dovuta all’incapacità di un particolare tipo di cellule gliali, gli oligodendrociti, di produrre la mielina. Nello specifico, sto studiando il modo in cui gli oligodendrociti si formano durante lo sviluppo perché nei pazienti con Huntington abbiamo osservato un blocco nel differenziamento.
Il ruolo delle cellule gliali nella malattia di Huntington è stato scoperto solo recentemente, in passato si guardava più al danno neuronale; oggi si è dimostrato un loro coinvolgimento anche in malattie prima insospettabili come la schizofrenia, l’Alzheimer e altri disturbi caratterizzati da deficit cognitivi.
A cosa è dovuto il blocco dello sviluppo degli oligodendrociti?
Il differenziamento cellulare è controllato da vari fattori epigenetici che rendono la cromatina più o meno accessibile per la trascrizione. Nel caso dell’Huntington vogliamo dimostrare che il blocco nel differenziamento è dovuto a un mancato srotolamento della cromatina in corrispondenza di geni fondamentali per la produzione della mielina. Si tratta in particolare dei geni OLIG2 (oligodendrocyte transcription factor 2) e SOX10, che sono fattori di trascrizione responsabili dell’attivazione dei geni produttori di mielina MBP (myelin basic protein) e PLP1 (proteolipid protein 1).
Il mancato srotolamento potrebbe essere dovuto alla huntingtina mutata che, interagendo con il DNA, ne altera a tal punto la struttura da rendere la cromatina inaccessibile agli enzimi della trascrizione.
Come si valuta lo stato della cromatina?
Uso una tecnica che si chiama ATAC Seq (Assay for Transposase-Accessible Chromatin using sequencing) che si basa sull’uso dell’enzima trasposasi: questo enzima taglia la cromatina nei punti in cui è accessibile e vi inserisce sequenze di DNA (trasposoni). Quando sequenziamo il genoma, andiamo a vedere in quali zone sono presenti queste sequenze tutte attaccate e identifichiamo la posizione in cui la cromatina era aperta per la trascrizione. A questo punto mappiamo i vari picchi e valutiamo su quali promotori si trovano e quali geni sono pronti per la trascrizione.
Un altro esperimento che facciamo consiste nel misurare la metilazione dei siti CpG, regioni di DNA in cui i residui di citosina sono vicini a quelli di guanina: se questi siti sono metilati, il DNA non è accessibile per la trascrizione. In pratica funziona in maniera opposta rispetto all’ATAC Seq, perciò se in un promotore non c’è il picco nell’ATAC Seq in genere vediamo un aumento della metilazione nelle CpG.
Un terzo tipo di strumento che utilizziamo è l’analisi del trascrittoma.
Alla fine usiamo la bioinformatica per integrare questi tre gruppi di informazione e facciamo uno studio comparativo tra due tipi di cellule gliali, normali e con la mutazione nella huntingtina. Gli oligodendrociti che usiamo derivano da cellule staminali embrionali, normali e mutate, indotte a diventare gliali con un protocollo di differenziamento che dura sei mesi.
Quando confrontiamo i dati di ATAC Seq, metilazione e trascrittoma si possono avere vari casi, quelli più ovvi prevedono un picco in ATAC Seq, un aumento della trascrizione di RNA e niente metilazione delle CpG; il caso opposto è nessun picco in ATAC Seq, alta metilazione e trascrizione assente. Può anche succedere che, pur non un avendo un segnale definito in ATAC Seq o nella metilazione del DNA, l’RNA sia comunque downregolato. In questo caso ci deve essere qualche altro meccanismo che reprime la trascrizione. Di solito si tratta di modificazioni a carico degli istoni, cioè quelle proteine che tengono il DNA compatto: la metilazione degli istoni, per esempio, può impedire l’accessibilità della cromatina ai fattori di trascrizione.
Quali sono le prospettive future del tuo lavoro?
Vorrei cominciare a usare cellule staminali derivate dalla riprogrammazione di fibroblasti provenienti da pazienti affetti da Huntington. Si parla di IPSC, induced pluripotent stem cells, e sono diffusissime anche in Italia: in pratica si preleva un campione di pelle dai pazienti con Huntington e, tramite un cocktail di quattro fattori di trascrizione (chiamato cocktail di Yamanaka), si convertono i fibroblasti in cellule staminali vere e proprie. A questo punto si stimola il differenziamento verso oligodendrociti. La cosa interessante è che queste cellule provengono da pazienti che hanno la mutazione nella huntingtina ma hanno sviluppato sintomi cognitivi e mostrano perdita di sostanza bianca anni prima dei sintomi motori.
Infine, una cosa più complessa che mi piacerebbe provare è una ChIP-seq della huntingtina mutata per trovare i siti di legame tra la proteina e il DNA. Si tratta di un’immunoprecipitazione, quindi una tecnica basata sul riconoscimento della huntingtina da parte di anticorpi, seguita dal sequenziamento dei frammenti di DNA che si legano a essa.
Segui Luisa Alessio su Twitter
Leggi anche: Colpire i tumori a intestino e cervello con l’epigenetica
Pubblicato con licenza Creative Commons Attribuzione-Non opere derivate 2.5 Italia. ![]()