 Riprodotto in laboratorio il primo anello della catena di reazioni chimiche responsabili della formazione del buco dell’ozono. La ricerca, recentemente pubblicata sulla rivista americana Science, nasce da una collaborazione tra INFM-CNR, Università di Sassari e Università di Bochum e potrebbe spiegare anche la formazione di molecole nello spazio interstellare.
Riprodotto in laboratorio il primo anello della catena di reazioni chimiche responsabili della formazione del buco dell’ozono. La ricerca, recentemente pubblicata sulla rivista americana Science, nasce da una collaborazione tra INFM-CNR, Università di Sassari e Università di Bochum e potrebbe spiegare anche la formazione di molecole nello spazio interstellare.
In un laboratorio grande quanto una goccia è stato individuato uno dei primi passi della sequenza di reazoni chimiche che porta alla formazione del buco dell’ozono. La reazione chimica che spiega l’assottigliarsi dello strato di ozono in atmosfera è nota da tempo agli scienziati; mancava però il primo anello di questa catena, ovvero la dissociazione di molecole di acido cloridico che favorisce la creazione di cloro responsabile poi della scomparsa dell’ozono.
Queste reazioni chimiche avvengono nella stratosfera, lo strato di atmosfera che inizia dodici chilometri sopra le nostre teste, dove la temperatura è estremamente bassa e in particolare nella lunga notte polare, sopra l’Antartide, può scendere fino a -80 °C. Proprio questo freddo è stato l’ostacolo che impediva la comprensione della formazione del buco dell’ozono alle sue origini. Il valore basso di questa temperatura, infatti, si traduce in bassi valori di energia termica delle molecole, energia indispensabile perché queste partecipino alle reazioni chimiche.
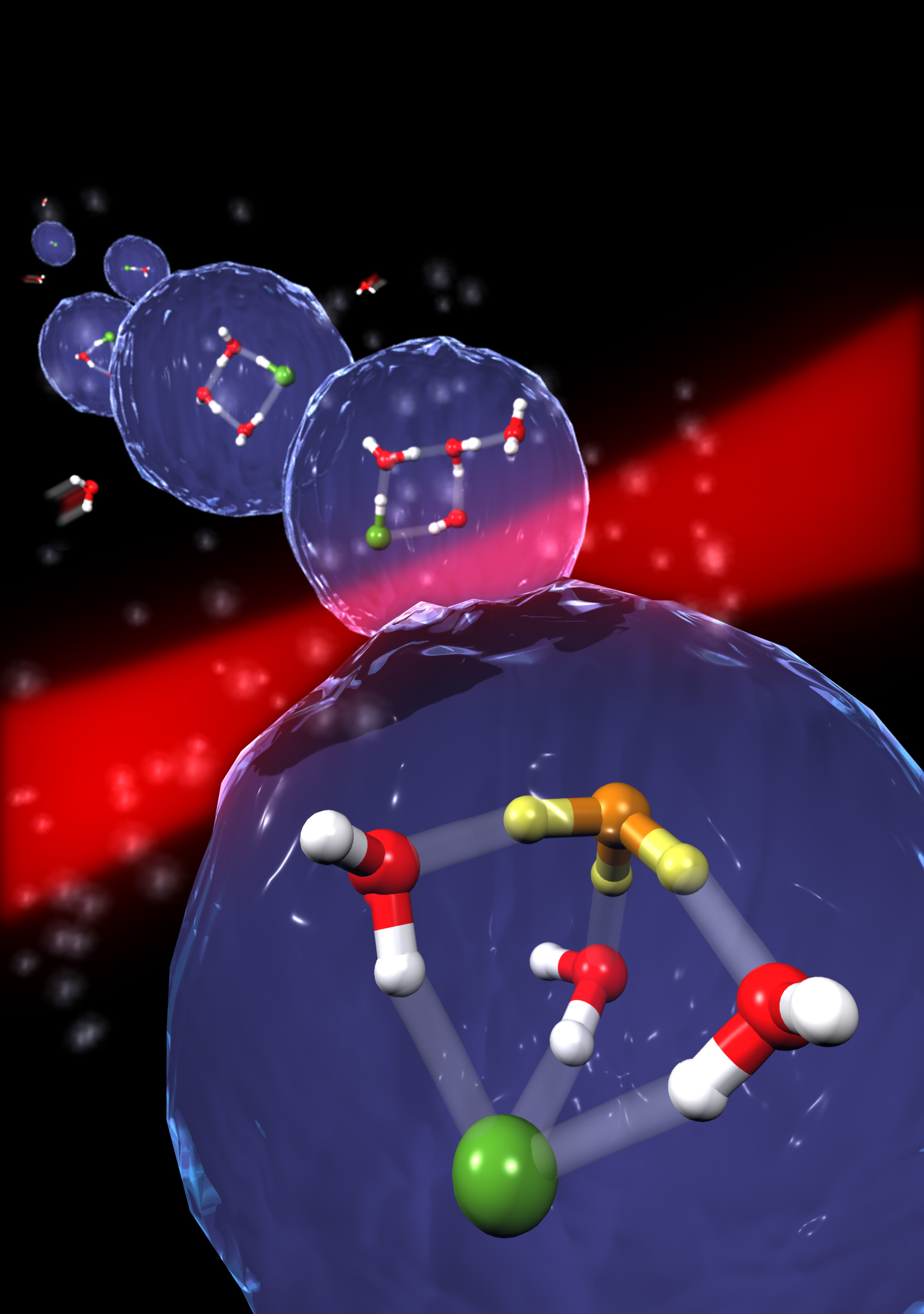
Per risolvere l’enigma, i ricercatori della INFM-CNR, dell’Università di Sassari e dell’Università di Bochum hanno studiato la reazione osservando molecole piccolissime, le più piccole unità chimiche in grado di prendere parte a reazioni, dette anche nanoaggregati. E’ stato possibile vedere questi oggetti microscopici grazie a una nuova tecnica che permette di catturare in una goccia di elio i nanoaggregati che partecipano alle reazioni. Questa tecnica, la spettroscopia infrarossa in elio superfluido, trasforma la goccia di elio in una sorta laboratorio microscopico dove i ricercatori possono misurare la massa e le interazioni delle molecole che vi sono intrappolate,; portando questo microlaboratorio quasi allo zero assoluto di temperatura, cioè raffreddandolo al di sotto dei -272°, i ricercatori hanno finalmente potuto osservare in diretta la dissoluzione dell’acido.





